Đề 6: Luyện thi THPTQG môn Hóa năm 2018
Đề 6: Luyện thi TPPTQG môn Hóa năm 2018. Đề gồm 40 câu hỏi, các em học sinh làm trong thời gian 50 phút. Khi làm xong, các em sẽ biết số điểm của mình và đáp án các câu hỏi. Hãy nhấn chữ bắt đầu ở phía dưới.
Câu 1: Các số oxi hóa đặc trưng của crom là:
- A. +2; +4; +6
- B. +1; +2; +4; +6
- C. +3; +4; +6
- D. +2; +3; +6
Câu 2: Nước muối sinh lí để sát trùng, rửa vết thương trong y học có nồng độ
- A. 0,9%
- B. 1%
- C. 1%
- D. 5%
Câu 3: Trong công nghiệp, người ta thường điều chế N2 từ
- A. amoni nitrat.
- B. không khí.
- C. axit nitric.
- D. amoniac.
Câu 4: Chất không thủy phân trong môi trường axit là
- A. tinh bột.
- B. glucozo.
- C. saccarozo.
- D. xenlulozo.
Câu 5: Thủy phân este nào sau đây không thu được sản phẩm có phản ứng tráng bạc?
- A. CH3COOCH3
- B. CH3COOCH=CH2
- C. HCOOCH3
- D. HCOOCH=CH2
Câu 6: Chất không dẫn điện được là
- A. KCl rắn, khan.
- B. NaOH nóng chảy.
- C. CaCl2 nóng chảy.
- D. HBr hòa tan trong nước.
Câu 7: Dãy kim loại bị thụ động trong axit HNO3 đặc, nguội là:
- A. Fe, Al, Cu.
- B. Fe, Al, Ag.
- C. Fe, Zn, Cr.
- D. Fe, Al, Cr.
Câu 8: Polime được điều chế bằng phản ứng trùng hợp là
- A. nilon-6,6.
- B. poli(etylen-terephtalat).
- C. xenlulozo triaxetat.
- D. polietilen.
Câu 9: Nước cứng có chứa nhiều các ion:
- A. K+, Na+.
- B. Zn2+, Al3+.
- C. Cu2+, Fe2+.
- D. Ca2+, Mg2+.
Câu 10: Trong số các kim loại sau: Ag, Cu, Au, Al. Kim loại có độ dẫn điện tốt nhất ở điều kiện thường là
- A. Al.
- B. Au.
- C. Ag.
- D. Cu.
Câu 11: Chất nào sau đây là hiđrocacbon?
- A. C2H5NH2.
- B. CH3COOH.
- C. C2H5OH.
- D. C2H6.
Câu 12: Tên của quặng chứa FeCO3, Fe2O3, Fe3O4, FeS2 lần lượt là:
- A. hematit, pirit, manhetit, xiđerit.
- B. xiđerit, manhetit, pirit, hematit.
- C. pirit, hematit, manhetit, xiđerit.
- D. xiđerit, hematit, manhetit, pirit.
Câu 13: Cho các chất sau: etilen, axetilen, buta-1,3-đien, benzen, toluen, stiren, metyl metacrylat. Số chất làm nhạt màu nước brom ở điều kiện thường là
- A. 6
- B. 5
- C. 7
- D. 4
Câu 14: Các dung dịch riêng biệt: Na2CO3, BaCl2, FeCl2, H2SO4, NaOH được đánh số ngẫu nhiên (1), (2), (3), (4), (5). Tiến hành một số thí nghiệm, kết quả ghi lại trong bảng sau:
Dung dịch | (1) | (2) | (4) | (5) |
(1) | Khí thoát ra | Có kết tủa | ||
(2) | Khí thoát ra | Có kết tủa | Có kết tủa | |
(4) | Có kết tủa | Có kết tủa | ||
(5) | Có kết tủa |
Các dung dịch (1), (3), (5) lần lượt là:
- A. H2SO4, FeCl2, BaCl2.
- B. Na2CO3, NaOH, BaCl2.
- C. H2SO4, NaOH, FeCl2.
- D. Na2CO3, FeCl2, BaCl2.
Câu 15: Cho sơ đồ phản ứng:
(1) X (C5H8O2) + NaOH → X1 (muối) + X2
(2) Y (C5H8O2) + NaOH → Y1 (muối) + Y2
Biết X1 và Y1 có cùng số nguyên tử cacbon; X1 có phản ứng với nước brom, còn Y1 thì không. X2 và Y2 có tính chất hóa học giống nhau là
- A. bị khử bởi H2 (to, Ni).
- B. bị oxi hóa bởi O2 (xúc tác) thành axit cacboxylic.
- C. tác dụng được với Na.
- D. tác dụng được với dung dịch AgNO3/NH3 (to).
Câu 16: Tiến hành thí nghiệm như hình vẽ:

Ban đầu trong cốc chứa nước vôi trong. Sục rất từ từ CO2 vào cốc cho tới dư. Hỏi độ sáng của bóng đèn thay đổi như thế nào?
- A. Giảm dần đến tắt rồi lại sáng tăng dần.
- B. Tăng dần rồi giảm dần đến tắt.
- C. Tăng dần.
- D. Giảm dần đến tắt.
Câu 17: Khi đốt cháy than đá, thu được hỗn hợp khí trong đó có khí X (không màu, không mùi, độc). Khí X là
- A. CO2.
- B. SO2.
- C. CO.
- D. NO2.
Câu 18: Dung dịch X có chứa 0,3 mol Na+; 0,1 mol Ba2+; 0,05 mol Mg2+; 0,2 mol Cl- và x mol NO3-. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là
- A. 44,4.
- B. 48,9.
- C. 68,6.
- D. 53,7.
Câu 19: Phát biểu nào sau đây không đúng?
- A. Đốt cháy a mol triolein thu được b mol CO2 và c mol H2O, trong đó b-c=6a.
- B. Etyl fomat làm mất màu dung dịch nước brom và có phản ứng tráng bạc.
- C. Đốt cháy hoàn toàn hỗn hợp gồm metyl axetat và etyl axetat luôn thu được số mol CO2 bằng số mol H2O.
- D. Tripanmitin, tristearin đều là chất rắn ở điều kiện thường.
Câu 20: Có các chất sau: Na2O, NaCl, Na2CO3, NaNO3, Na2SO4. Có bao nhiêu chất mà bằng một phản ứng có thể tạo ra NaOH?
- A. 2
- B. 4
- C. 3
- D. 5
Câu 21: Tiến hành thí nghiệm với các chất X, Y, Z, T, kết quả được trình bày trong bảng dưới đây:
X | Y | Z | T | |
Nước brom | Không mất màu | Mất màu | Không mất màu | |
Nước | Tách lớp | Tách lớp | Dung dịch đồng nhất | |
Dung dịch AgNO3/NH3 | Không có kết tủa | Có kểt tủa | Có kểt tủa | Không có kết tủa |
X, Y, Z, T lần lượt là:
- A. axit aminoaxetic, glucozo, fructozo, etyl axetat.
- B. etyl axetat, glucozo, axit aminoaxetic, fructozo.
- C. etyl axetat, glucozo, fructozo, axit aminoaxetic.
- D. etyl axetat, fructozo, glucozo, axit aminoaxetic.
Câu 22: Cho dãy các chất: H2NCH2COOH, H2NCH2CONHCH(CH3)COOH, CH3COONH3C2H5, C6H5NH2, CH3COOH. Số chất trong dãy phản ứng được với dung dịch NaOH và HCl là
- A. 2
- B. 3
- C. 5
- D. 4
Câu 23: Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2 (đktc) được giải phóng là
- A. 4,48 lít.
- B. 8,19 lít.
- C. 7,33 lít.
- D. 6,23 lít.
Câu 24: Cho m gam glucozo tác dụng với lượng dư dung dịch AgNO3/NH3 thu được 86,4 gam Ag. Nếu lên men hoàn toàn m gam glucozo rồi cho khí CO2 thu được hấp thụ vào nước vôi trong dư thì lượng kết tủa thu được là
- A. 60 gam.
- B. 40 gam.
- C. 80 gam.
- D. 20 gam.
Câu 25: Hỗn hợp X gồm 0,15 mol Mg và 0,1 mol Fe cho vào 500 mol dung dịch Y gồm AgNO3 và Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn, thu được 20 gam chất rắn Z và dung dịch E. Cho dung dịch NaOH dư vào dung dịch E, lọc kết tủa và nung ngoài không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp 2 oxit. Nồng độ mol/l của AgNO3 và Cu(NO3)2 lần lượt là
- A. 0,12M và 0,3M.
- B. 0,24M và 0,5M.
- C. 0,24M và 0,6M.
- D. 0,12M và 0,36M.
Câu 26: Cho 16,6 gam hỗn hợp X gồm metyl fomat và phenyl axetat (tỉ lệ mol tương ứng 1:2) tác dụng hoàn toàn với 200 ml dung dịch NaOH 1,5M thu được dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan. Giá trị của m là
- A. 28,6
- B. 25,2
- C. 23,2
- D. 11,6
Câu 27: Hỗn hợp X gồm etilen và hiđro có tỉ khối so với hiđro là 4,25. Dẫn X qua Ni nung nóng được hỗn hợp Y (hiệu suất 75%). Tỉ khối của Y so với hiđro là
- A. 5,52
- B. 6,20
- C. 5,23
- D. 5,80
Câu 28: X có công thức C4H14O3N2. Khi cho X tác dụng với dung dịch NaOH thì thu được hỗn hợp Y gồm 2 khí ở điều kiện thường và đều có khả năng làm xanh quỳ tím ẩm. Số công thức cấu tạo phù hợp của X là
- A. 3
- B. 5
- C. 4
- D. 2
Câu 29: Hòa tan hết 0,54 gam Al trong 70 ml dung dịch HCl 1M, thu được dung dịch X. Cho 75 ml dung dịch NaOH 1M vào X, sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
- A. 0,78.
- B. 1,17.
- C. 1,56.
- D. 0,29.
Câu 30: Cho m gam hỗn hợp X gồm Ba, BaO, Ba(OH)2 có cùng số mol vào nước, thu được 500 ml dung dịch Y và a mol H2. Hấp thụ từ từ 3,6a mol CO2 vào 500 ml dung dịch Y, kết quả thí nghiệm được biểu diễn bằng đồ thị sau:
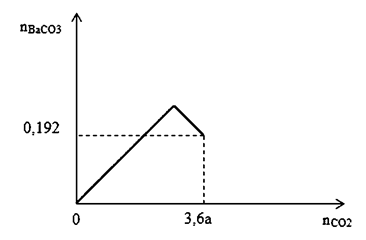
- A. 46,10.
- B. 32,27.
- C. 36,88.
- D. 41,49.
Câu 31: Hỗn hợp X gồm Mg, MgO, Ca và CaO. Hòa tan 10,72 gam X vào dung dịch HCl vừa đủ, thu được 3,248 lít khí (đktc) và dung dịch Y. Trong Y có 12,35 gam MgCl2 và m gam CaCl2. Giá trị của m là
- A. 19,98.
- B. 33,3.
- C. 13,32.
- D. 15,54.
Câu 32: Hòa tan hết 20 gam hỗn hợp X gồm Cu và các oxit sắt (trong hỗn hợp X oxi chiếm 16,8% về khối lượng) cần vừa đủ dung dịch hỗn hợp A chứa b mol HCl và 0,2 mol HNO3 thu được 1,344 lít NO (đktc) là sản phẩm khử duy nhất và dung dịch Y. Cho dung dịch Y tác dụng với một lượng AgNO3 vừa đủ thu được m gam kết tủa và dung dịch Z. Cho Z tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa, nung đến khối lượng không đổi thu được 22,4 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
- A. 76,81.
- B. 70,33.
- C. 78,97.
- D. 83,29.
Câu 33: Lấy m gam hỗn hợp bột Al và Fe2O3 đem phản ứng nhiệt nhôm. Để nguội sản phẩm sau đó chia thành hai phần không đều nhau. Phần 1 cho tác dụng với dung dịch NaOH dư, thu được 8,96 lít khí H2 (đktc) và phần không tan có khối lượng bằng 44,8% khối lượng phần 1. Phần 2 hòa tan hoàn toàn trong dung dịch HCl thu được 2,688 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
- A. 57,5.
- B. 50,54.
- C. 83,21.
- D. 53,2.
Câu 34: Xà phòng hóa hoàn toàn m gam một este no, đơn chức, mạch hở E bằng 26 gam dung dịch MOH 28% (M là kim loại kiềm). Cô cạn hỗn hợp sau phản ứng thu được 24,72 gam chất lỏng X và 10,08 gam chất rắn khan Y. Đốt cháy hoàn toàn Y, thu được CO2, H2O và 8,97 gam muối cacbonat khan. Mặt khác, cho X tác dụng với Na dư, thu được 12,768 lít khí H2 (đktc). Phần trăm khối lượng muối trong Y có giá trị gần nhất với
- A. 85,0
- B. 85,5
- C. 84,0
- D. 83,0
Câu 35: Cho hỗn hợp gồm Cu2S và FeS2 tác dụng hết với dung dịch chứa 0,52 mol HNO3, thu được dung dịch X (không chứa NH4+) và hỗn hợp khí gồm NO và 0,3 mol NO2. Để tác dụng hết với các chất trong X cần dùng 260 ml dung dịch NaOH 1M, sau phản ứng lọc kết tủa nung trong không khí tới khối lượng không đổi thu được 6,4 gam chất rắn. Tổng khối lượng chất tan có trong dung dịch X gần nhất với giá trị nào sau đây?
- A. 21,0
- B. 19,0
- C. 18,0
- D. 20,0
Câu 36: Đốt cháy este 2 chức mạch hở X (được tạo từ axit cacboxylic no, đa chức, phân tử X không có quá 5 liên kết π) thu được tổng thể tích CO2 và H2O gấp 5/3 lần thể tích O2 cần dùng. Lấy 21,6 gam X tác dụng hoàn toàn với 400 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được m gam chất rắn. Giả trị lớn nhất của m là
- A. 28,0.
- B. 24,8.
- C. 24,1.
- D. 26,2.
Câu 37: Hỗn hợp X gồm Na2SO3, CuO, CuCO3,. Hòa tan m gam hỗn hợp X trong dung dịch hỗn hợp HCl 1M và H2SO4 0,5M vừa đủ, thu được dung dịch Y chứa (m+8,475) gam chất tan gồm muối clorua và sunfat trung hòa; 5,6 lít hỗn hợp khí (đktc) có tỉ khối so với hidro là 27,6. Điện phân dung dịch Y với điện cực trơ, màng ngăn xốp đến khi lượng Cu2+ còn lại bằng 6% lượng Cu2+ trong dung dịch Y thì dừng lại thu được dung dịch Z. Cho 0,14m gam Fe vào dung dịch Z đến khi phản ứng kết thúc thu được m1 gam chất rắn. Giá trị của m1 là
- A. 4,9216.
- B. 4,5118.
- C. 4,6048.
- D. 4,7224.
Câu 38: Hòa tan hoàn toàn 5,22 gam hỗn hợp bột M gồm Mg, MgO, Mg(OH)2, MgCO3, Mg(NO3)2 bằng một lượng vừa đủ 0,26 mol HNO3. Sau khi phản ứng kết thúc thu được dung dịch X và 0,448Đề 3: Luyện thi TPPTQG môn Hóa năm 2018. Đề gồm 40 câu hỏi, các em học sinh làm trong thời gian 50 phút. Khi làm xong, các em sẽ biết số điểm của mình và đáp án các câu hỏi. Hãy nhấn chữ bắt đầu ở phía dưới. lít hỗn hợp khí gồm N2O và CO2. Dung dịch X phản ứng vừa đủ với 250 ml dung dịch NaOH 1M, sau phản ứng thu được 6,96 gam kết tủa màu trắng. Phần trăm theo khối lượng của Mg(OH)2 trong hỗn hợp đầu gần nhất là
- A. 44,44%
- B. 22,22%
- C. 11,11%
- D. 33,33%
Câu 39: Cho hỗn hợp X chứa hai peptit M và Q đều tạo bởi hai amino axit đều no, chứa 1 nhóm –COOH và 1 nhóm –NH2. Tổng số nguyên tử O của M và Q là 14. Trong M hoặc Q đều có số liên kết peptit không nhỏ hơn 4. Cứ 0,25 mol X tác dụng hoàn toàn với KOH (đun nóng) thì thấy có 1,65 mol KOH phản ứng và thu được m gam muối. Mặt khác, đốt cháy hoàn toàn 54,525 gam X rồi cho sản phẩm hấp thụ hoàn toàn vào bình chứa Ba(OH)2 dư thấy khối lượng bình tăng 120,375 gam. Giá trị của m là
- A. 187,25.
- B. 196,95.
- C. 226,65.
- D. 213,75.
Câu 40: Đun nóng m gam hỗn hợp X gồm glyxin và alanin thu được m1 gam hỗn hợp Y gồm các đipepetit mạch hở. Nếu đun nóng 2m gam X trên thu được m2 gam hỗn hợp Z gồm các tripeptit mạch hở. Đốt cháy hoàn toàn m1 gam Y thu được 0,72 mol H2O; nếu dốt cháy hoàn toàn m2 gam Z thì thu được 1,34 mol H2O. Giá trị của m là
- A. 24,18 gam
- B. 24,60 gam
- C. 24,74 gam
- D. 24,46 gam
Xem thêm bài viết khác
- Lời giải câu số 2, 6, 32 Đề thi thử THPT quốc gia môn Hóa lần 1 năm 2017 của trường THPT chuyên KHTN
- Lời giải câu số 26, 32, 35 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 6
- Đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 9
- Đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 5
- Thi THPTQG 2020: Đề thi và đáp án môn Hóa học mã đề 224
- Lời giải câu số 4, 6, 10 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 6
- Thi THPTQG 2019: Đề thi và đáp án môn Hóa học mã đề 209
- Lời giải câu số 30, 3, 40 Đề thi thử THPT quốc gia môn Hóa lần 3năm 2017 của trường THPT chuyên ĐH Vinh
- Lời giải câu số 9, 26, 30 Đề thi thử THPT quốc gia môn Hóa năm 2017 của trường THPT chuyên ĐHSP
- Lời giải câu số 17,20, 27 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 14
- Đề và đáp án môn Hóa học mã đề 211 thi THPT quốc gia năm 2017 đáp án của bộ GD-ĐT
- Cách làm câu số 4, 5, 16 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 23











