Giải câu 5 bài 10: Một số muối quan trọng
Câu 5.(Trang 36 SGK)
Trong phòng thí nghiệm có thể dùng những muối KClO3 hoặc KNO3 để điều chế khí oxi bằng phản ứng phân hủy.
a) Viết các phương trình hóa học đối với mỗi chất.
b) Nếu dùng 0,1 mol mỗi chất thì thể tích khí oxi thu được có khác nhau hay không? Hãy tính thể tích khí oxi thu được.
c) Cần điều chế 1,12 lít khí oxi, hãy tính khối lượng mỗi chất cần dùng.
Các thể tích khí được đo ở điều kiện tiêu chuẩn.
Bài làm:
a) Phương trình hóa học điều chế khí oxi:
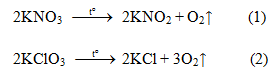
b) Nếu dùng 0,1 mol mỗi chất thì
Từ (1): nO2 = 1/2 nKNO3 = 1/2.0,1 = 0,05 mol; VO2 = 0,05x22,4 = 1,12 lít
Từ (2): nO2 = 3/2.nKClO3 = 3/2.0,1 = 0,15 mol; VO2 = 0,15x22,4 = 3,36 lít
Vậy với cùng một số mol bị nhiệt phân thì thể tích khí O2 thu được từ KClO3 nhiều hơn
c) Điều chế 1,12 lít khí O2, nO2 = 1,12/22,4 = 0,05 mol
Từ (1): nKNO3 = 2nO2 = 0,1 mol; =>mKNO3 = 0,1x101 = 10,1 g
Từ (2): nKClO3 = 2/3nO2 = 2/3.0,05 mol; =>VKClO3 = 2/3.0,05.122,5 = 4,086 g.
Xem thêm bài viết khác
- Giải câu 4 bài 29: Axit cacbonic và muối cacbonat
- Giải câu 3 bài 22: Luyện tập chương 2 Kim loại
- Giải bài 24 hóa học 9: Ôn tập học kì 1
- Giải bài 38 hoá học 9: Axetilen
- Giải câu 2 bài 7: Tính chất hóa học của bazơ
- Giải câu 6 bài 9: Tính chất hóa học của muối
- Giải bài 18 hóa học 9: Nhôm
- Giải bài 55 hóa học 9: Thực hành: Tính chất của gluxit
- Giải bài 56 hóa học 9: Ôn tập cuối năm Phần 1
- Giải câu 4 bài 14: Thực hành Tính chất hóa học của bazơ và muối
- Giải câu 4 bài 8: Một số bazơ quan trọng Tiết 2
- Giải câu 2 bài 21: Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn











