Lời giải câu số 2, 8, 30 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 7
Bài làm:
Lời giải câu số 2, 8, 30
Câu 2: Đáp án A
Đặt nFeS2 = a; nFeS = b ; nCu = c
Khi cho BaCl2 vào dung dịch X, ta có : nS = 0,12 = 2a + b (1)
Khi cho Ba(OH)2 dư vào dung dịch X, ta có khối lượng các hidroxit tạo thành là :
36,92 – 27,96 = (a + b).107 + 98c (2)
Lại có : 8,72 = 120a + 88b + 64c (3)
Giải (1), (2), (3), ta được a = 0,05; b = 0,02 ; c= 0,015
Áp dụng pp bảo toàn e, ta có: nHNO3 = 0,32 mol Suy ra nHNO3 dư = 1,6 – 0,32 = 1,28 mol
Khi đó, dung dịch X gồm HNO3 dư 1,28mol và Fe2(SO4)3 0,035mol và CuSO4 0,015mol
Suy ra số mol Cu bị hòa tan tối đa là :
nFe3+/2 + (3/8)nHNO3 dư = 0,515 mol
Vậy khối lượng Cu mà X có khả năng hòa tan tối đa là 32,96gam.
Vậy khối lượng quặng hemantit là 320kg.
Câu 8: Đáp án C
nCr = 7,8/52 = 0,15 mol =>nCrCl3 = 0,15 mol
=>nCl2 = (3/2)nCrCl3 = 0,255 mol
Vậy V = 5,04l
Câu 30: Đáp án D
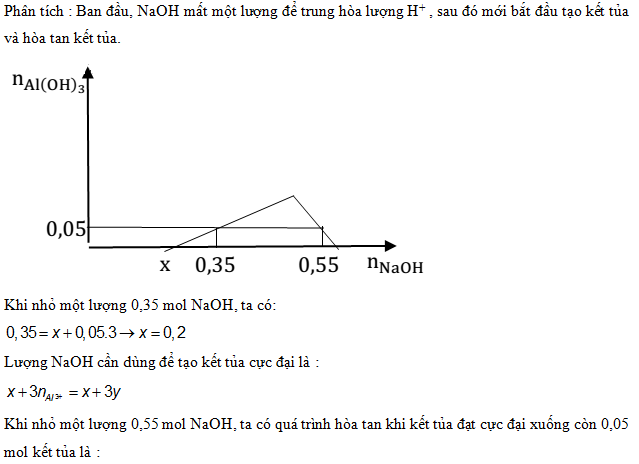
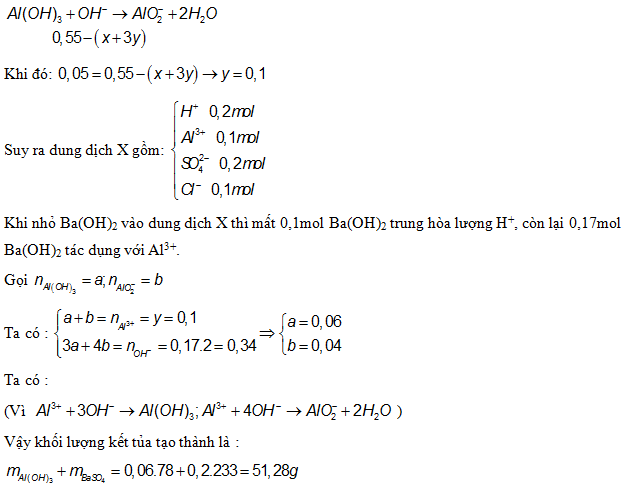
Xem thêm bài viết khác
- Lời giải câu số 29, 30, 33 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 8
- Lời giải câu số 9, 17, 32 Đề thi thử THPT quốc gia môn Hóa năm 2017 của trường THPT chuyên Lam Sơn Thanh Hóa
- Đề và đáp án môn Hóa học mã đề 209 thi THPT quốc gia năm 2017 đáp án của bộ GD-ĐT
- Đáp án Đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 4
- Đề và đáp án môn Hóa học mã đề 214 thi THPT quốc gia năm 2017 đáp án của bộ GD-ĐT
- Đề và đáp án môn Hóa học mã đề 218 thi THPT quốc gia năm 2017 đáp án của bộ GD-ĐT
- Đề thi thử THPT quốc gia môn Hóa năm 2017 của trường THPT chuyên ĐHSP
- Lời giải câu số 2, 6, 32 Đề thi thử THPT quốc gia môn Hóa lần 1 năm 2017 của trường THPT chuyên KHTN
- Lời giải câu số 1, 6, 29 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 7
- Thi THPTQG 2019: Đề thi và đáp án môn Hóa học mã đề 204
- Cách làm câu số 35, 36, 38 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 25
- Lời giải câu số 35, 36, 39 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 16











