Đề 2: Luyện thi THPTQG môn Hóa năm 2018
Đề 2: Luyện thi TPPTQG môn Hóa năm 2018. Đề gồm 40 câu hỏi, các em học sinh làm trong thời gian 50 phút. Khi làm xong, các em sẽ biết số điểm của mình và đáp án các câu hỏi. Hãy nhấn chữ bắt đầu ở phía dưới.
Câu 1. Thành phần chính của phân lân supephotphat kép là:
- A. Ca(H2PO4)2.CaSO4.
- B. Ca3(PO4)2.
- C. CaSO4.
- D. Ca(H2PO4)2.
Câu 2. Chất nào sau đây có phản ứng tráng bạc?
- A. C2H5OH.
- B. CH3NH2.
- C. HCOOH.
- D. CH3COOH.
Câu 3. Dãy các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối của chúng với điện cực trơ là:
- A. Ni, Cu, Ag.
- B. Cu, Ca, Zn.
- C. Li, Ag,Sn.
- D. Fe, Cr, Al.
Câu 4. Hòa tan Fe3O4 trong dung dịch H2SO4 loãng, dư thu được dung dịch X. Cho dung dịch X lần lượt phản ứng với các chất sau: KMnO4, Cl2, NaOH, Cu(NO3)2, Cu, KNO3, KI. Số phản ứng xảy ra là:
- A. 7.
- B. 4.
- C. 6.
- D. 5.
Câu 5. Hỗn hợp X chứa: NaHCO3, NH4NO3 và CaO (các chất có cùng số mol). Hòa tan hỗn hợp X vào H2O (dư), đun nóng. Sau phản ứng kết thúc, lọc bỏ kết tủa, thu được dung dịch Y. Dung dịch Y có môi trường:
- A. Axit.
- B. Lưỡng tính.
- C. Bazơ.
- D. Trung tính.
Câu 6. Có 4 dung dịch có cùng nồng độ mol là : (1) H2NCH2COOH, (2) CH3COOH, (3) CH3CH2NH2, (4) NH3. Dãy các dung dịch xếp theo thứ tự pH giảm dần là :
- A. (2)>(1)>(3)>(4).
- B. (3) >(4)>(1)>(2).
- C. (3)>(4)>(2)>(1).
- D. (4)>(3)>(1)>(2).
Câu 7. Thủy phân este X trong môi trường axit, thu được 2 chất hữu cơ Y và Z. Oxi hóa Y tạo ra sản phẩm là Z. Chất X không thể là :
- A. Isopropyl propionat.
- B. Etylen glicol oxalat.
- C. Etyl axetat.
- D. Vinyl axetat.
Câu 8. Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch X:
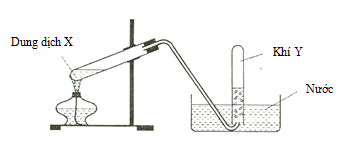
Hình vẽ trên minh họa phản ứng nào sau đây ?
- A. C2H5OH
 C2H4 + H2O.
C2H4 + H2O. - B. NaCl (rắn) + H2SO4(đặc)
 NaHSO4 + HCl.
NaHSO4 + HCl. - C. NH4Cl + NaOH
 NaCl + NH3 + H2O.
NaCl + NH3 + H2O. - D. CH3COONa (rắn) + NaOH(rắn)
 CH4 + Na2CO3.
CH4 + Na2CO3.
Câu 9.Hỗn hợp X gồm một anđehit và một ankin có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn a mol hỗn hợp X thu được 3a mol CO2 và 1,8a mol H2O. Hỗn hợp X có số mol 0,1 tác dụng được với tối đa 0,14 mol AgNO3 trong NH3 (điều kiện thích hợp). Số mol của anđehit trong 0,1 mol hỗn hợp X là :
- A. 0,02.
- B. 0,03.
- C. 0,01.
- D. 0,04.
Câu 10. Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol đồng đẳng kế tiếp, cho sản phẩm cháy qua bình chứa dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 19,1 gam và có 25 gam kết tủa. Nếu oxi hóa hết m gam X bằng CuO dư, lấy sản phẩm thu được cho tác dụng với dung dịch AgNO3/ NH3 dư, đun nóng được x gam Ag. Giá trị của x là ( Coi hiệu suất là 100%):
- A. 64,8.
- B. 75,6.
- C. 43,2.
- D. 86,4.
Câu 11. Cho 66,2 gam hỗn hợp X gồm Fe3O4, Fe(NO3)2, Al tan hoàn toàn trong dung dịch chứa 3,1 mol KHSO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 466,6 gam muối sunfat trung hòa và 10,08 lít (đktc) khí Z gồm 2 khí, trong đó có một khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với He là ![]() . Phần trăm khối lượng của Al trong hỗn hợp gần nhất với giá trị nào sau đây:
. Phần trăm khối lượng của Al trong hỗn hợp gần nhất với giá trị nào sau đây:
- A. 30.
- B. 15.
- C. 25.
- D. 20.
Câu 12. Có các nhận định sau :
(a) Protein có phản ứng màu biure.
(b) Tất cả các protein đều tan trong nước tạo thành dung dịch keo.
(c) Protein bị thủy phân nhờ xúc tác axit, bazơ hoặc ezim tạo thành các
- amino axit.(d) Đipeptit phản ứng với Cu(OH)2/OH- cho phức chất có màu tím đặc trưng.
(e) Khi nhỏ dung dịch HNO3 đặc vào lòng trắng trứng, thấy xuất hiện kết tủa màu vàng.
Số nhận định đúng là:
- A. 5.
- B. 1
- C. 3.
- D. 2.
Câu 13. Cho phản ứng : FeO + HNO3 → Fe(NO3)3 + NO + H2O
Tỉ lệ số phân tử HNO3 đóng vai trò là chất oxi hóa và môi trường trong phản ứng là bao nhiêu?
- A. 1 : 9.
- B. 1 : 3.
- C. 1 : 2.
- D. 1 : 10.
Câu 14. Hỗn hợp E gồm peptit X mạch hở (cấu tạo từ Gly, Ala) và este Y (được tạo ra từ phản ứng este hóa giữa axit cacboxylic no, đơn chức và metanol). Đốt cháy hoàn toàn m gam E cần 15,68 lít O2 (đktc). Mặt khác, khi thủy phân m gam E trong dung dịch NaOH vừa đủ thu được 24,2 gam hỗn hợp muối (trong đó số mol muối natri của Gly lớn hơn số mol muối của Ala). Đốt cháy hoàn toàn lượng muối trên cần 20 gam O2, thu được Na2CO3, N2, H2O và 18,7 gam CO2. Tỉ lệ số mol Gly : Ala trong X là:
- A. 3 : 1.
- B. 1 : 2.
- C. 1 : 3.
- D. 1 : 1.
Câu 15. Các nhận xét sau:
(a) Thành phần chính của phân đạm ure là (NH2)2CO.
(b) Phân đạm amoni nên bón cho loại đất chua.
(c) Tro thực vật cũng là một loại phân kali vì có chứa K2CO3.
(d) Độ dinh dưỡng của phân lân được đánh giá bằng phần trăm khối lượng photpho.
(e) NPK là một loại phân bón hỗn hợp.
(f) Người ta dùng loại phân bón chứa nguyên tố kali để tăng cường sức chống bệnh, chống rét và chịu hạn cho cây.
Số nhận xét sai là:
- A. 3.
- B. 1.
- C. 2.
- D. 4.
Câu 16. Cho các chất : Cu(NO3)2, AgNO3, Fe(NO3)2, MgCO3, NH4NO3, Ba(HCO3)2 và NH4HCO3 . Nếu nung các chất trên đến khối lượng không đổi trong các bình kín không có không khí, rồi cho nước vào các bình. Số bình có thể tạo lại chất ban đầu sau các thí nghiệm là:
- A. 4.
- B. 5.
- C. 2.
- D. 3.
Câu 17. Cho ancol : H3C- CH-CH2 - CH2- CH2 – OH Tên nào dưới đây ứng với ancol trên ?
- A. 4-metylpentan-2-ol.
- B. 2-metylpentan-1-ol.
- C. 3-metylhexan-2-ol.
- D. 4-metylpentan-1-ol.
Câu 18. Trong số các nguồn năng lượng: (1)thủy điện, (2) gió, (3)mặt trời, (4) hóa thạch; Những nguồn năng lượng sạch là:
- A. (2), (3), (4).
- B. (1), (3),(4) .
- C. (1), (2),(4).
- D. (1), (2),(3) .
Câu 19. Cho dãy chất: Al, Al(OH)3, Al2O3, AlCl3. (NH4)2CO3, CH3COONH4, NaHCO3. Số chất có tính chất lưỡng tính là:
- A. 6.
- B. 2.
- C. 5.
- D. 7.
Câu 20. Amino axit X có công thức (H2N)2C3H5COOH. Cho 0,02 mol X tác dụng với 200 ml dung dịch hỗn hợp H2SO4 0,1M và HCl 0,3M, thu được dung dịch Y. Cho Y phản ứng vừa đủ với 400 ml dung dịch NaOH 0,1M và KOH 0,2M, thu được dung dịch chứa m gam muối. Giá trị của m là:
- A. 8,09.
- B. 10,43.
- C. 6,38.
- D. 10,45.
Câu 21. Cho sơ đồ phản ứng: NaCl (X) NaHCO3 (Y) NaNO3. X và Y có thể là:
- A. NaOH và NaClO.
- B. Na2CO3 và NaClO.
- C. NaClO3 và Na2CO3.
- D. NaOH và Na2CO3.
Câu 22. Trong bệnh viện, nhiều bệnh nhân thường được truyền dịch đường để bổ sung năng lượng một cách nhanh nhất. Chất trong dịch truyền có tác dụng trên là:
- A. Mantozơ.
- B. Saccarozơ.
- C. Fructozơ.
- D. Glucozơ.
Câu 23. Đốt cháy hoàn toàn a gam S rồi cho sản phẩm sục qua 200 ml dung dịch NaOH bM thu được dung dịch X. Chia X làm hai phần bằng nhau. Phần 1 cho tác dụng với dung dịch CaCl2 dư thấy xuất hiện c gam kết tủa. Phần 2 tác dụng với dung dịch nước vôi trong dư thấy xuất hiện d gam kết tủa. Biết d > c. Có bao nhiêu kết quả không chính xác trong số kết quả sau:
(a) ![]()
(b) 3,2b < a < 6,4b
(c) a > 6,4b
(d) a < 3,2b
- A. 1.
- B. 3.
- C. 2.
- D. 4.
Câu 24. Cho 19,45 gam hỗn hợp X gồm Na và Ba vào 75ml dung dịch Al2(SO4)3 1M thu được 5,04 lít khí H2 (đktc), dung dịch A và m gam kết tủa. Giá trị của m là:
- A. 11,7.
- B. 52,425.
- C. 35.
- D. 64,125.
Câu 25. Axit cacboxylic X hai chức (có phần trăm khối lượng của oxi nhỏ hơn 70%), Y và Z là hai ancol đồng đẳng kế tiếp (My < Mz). Đốt cháy hoàn toàn 0,2 mol hỗn hợp X, Y, Z cần vừa đủ 8,96 là khí O2 (đktc), thu được 7,84 lít khí CO2 (đktc) và 8,1 gam H2O. Phần trăm khối lượng của Y trong hỗn hợp trên gần nhất với giá trị nào sau đây?
- A. 29% .
- B. 12%.
- C. 25%.
- D. 15%
Câu 26: Cặp hợp chất không phản ứng được với nhau là
- A. Ag + FeCl3
- B. Fe + CuSO4
- C. Ca + H2SO4
- D. Cu + HNO3
Câu 27. Cho 12,0 gam axit axetic phản ứng với 6,9 gam etanol (xúc tác H2SO4 đặc, to) thu được m gam este. Biết hiệu suất phản ứng este hóa bằng 60%. Giá trị của m là :
- A. 7,8.
- B. 7,92.
- C. 9,72.
- D. 10,56.
Câu 28.Để 2,52 gam bột sắt trong không khí, sau một thời gian thu được 2,84 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4. Để hòa tan hết X cần 500 ml dung dịch HNO3 a (mol/l), sau phản ứng sinh ra 0,56 lít NO (sản phẩm khử duy nhất ở đktc) và dung dịch Y. Giá trị của a và khối lượng chất tan trong Y là:
- A. 0,25M và 6,95 gam.
- B. 0,028M và 9,65 gam.
- C. 0,28 M và 9,65 gam.
- D. 0,025M và 6,95 gam.
Câu 29. Cho các dung dịch: NaOH, HCl, Br2, C2H5OH. Số dung dịch trong dãy phản ứng được với phenol là:
- A. 4.
- B. 3.
- C. 1.
- D. 2.
Câu 30. Điện phân với điện cực trơ dung dịch chứa 0,3 mol AgNO3 với cường độ dòng điện 2,68 A, trong thời gian t (giờ) thu được dung dịch X . Cho 22,4 gam bột Fe vào dung dịch X, thu được khí NO (sản phẩm khử duy nhất của ) và 34,28 gam chất rắn. Các phản ứng xảy ra hoàn toàn và hiệu suất của quá trình điện phân là 100%. Giá trị của t là:
- A. 1,25.
- B. 1,20.
- C. 1,00.
- D. 1,40.
Câu 31. Chất nào sau đây phản ứng được với NaHCO3?
- A. Axit benzoic.
- B. Anđehit axetic.
- C. Phenol.
- D. Ancol bezylic.
Câu 32. Cho dung dịch KOH vào dung dịch hỗn hợp gồm a mol HCl và b mol CrCl3.
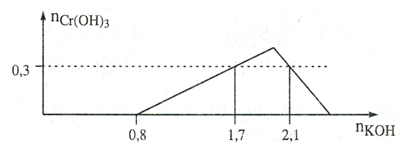
Tỉ lệ a : b là :
- A. 2 : 3.
- B. 1 : 2.
- C. 2 : 1.
- D. 3 : 2.
Câu 33. Cho 2,760 gam chất hữu cơ A (chứa C,H,O và có 100 < MA< 150) tác dụng với NaOH vừa đủ, sau đó làm khô, phần bay hơi chỉ có nước, phần chất rắn khan còn lại chứa hai muối của natri có khối lượng 4,440 gam. Nung nóng 2 muối trong oxi dư, sau khi phản ứng xảy ra hoàn toàn thu được 3,180 gam Na2CO3, 2,464 lít CO2 (ở đktc) và 0,900 gam nước. Công thức phân tử và số đồng phân cấu tạo của A là:
- A. C7H6O3; 3.
- B. C7H6O3; 2.
- C. C6H6O3; 2.
- D. C6H6O3; 3.
Câu 34. Khẳng định nào sau đây là sai?
- A. CaSO4.2H2O có trong tự nhiên, là thạch cao sống.
- B. Al(OH)3 là bazơ lưỡng tính.
- C. Nguyên tắc làm mềm nước cứng là giảm nồng độ Ca2+, Mg2+, trong nước.
- D. Nước cứng làm cho xà phòng ít bọt, giảm khả năng tẩy rửa của xà phòng.
Câu 35. Cho 23,06 gam hỗn hợp hai muối MgCO3 và RCO3 vào dung dịch H2SO4 loãng, thu được 0,896 lít khí CO2 (đktc), chất rắn X và dung dịch Y chứa 2,4 gam muối. Nung X đến khối lượng không đổi, thu được chất rắn Z và 2,24 lít khí CO2 (đktc). Khối lượng của Z là:
- A. 17,7 gam.
- B. 15,3 gam.
- C. 15,5 gam.
- D. 17,1 gam.
Câu 36. Cho sơ đồ chuyển hóa
![]()
Tên gọi của Y là:
- A. Glixerol.
- B. Propan -2-ol.
- C. Propan -1,2 – điol.
- D. Propan – 1,3 - điol.
Câu 37. Cho sơ đồ phản ứng:
X + Na[Al(OH)4] → M↓ + Y
Y + AgNO3
→ AgCl + ...X là:
- A. CO2.
- B. NH3.
- C. SO2.
- D. HCl.
Câu 38. Nung nóng m gam hỗn hợp X gồm bột Al và FexOy trong điều kiện không có không khí thu được hỗn hợp Y. Nghiền nhỏ, trộn đều hỗn hợp Y rồi chia thành 2 phần: Phần 1 có khối lượng 14,49 gam được hòa tan hết trong dung dịch HNO3 loãng, dư, đun nóng thu được dung dịch Z và 0,165 mol NO ( sản phẩm khử duy nhất ). Phần 2 đem tác dụng với dung dịch NaOH dư, đun nóng thu được 0,015 mol khí H2 và còn lại 2,52 gam chất rắn. Công thức của oxit sắt và giá trị của m lần lượt là:
- A. Fe2O3 và 28,98.
- B. Fe3O4 và 19,32.
- C. Fe3O4 và 28,98.
- D. FeO và 19,32.
Câu 39. Cho các phản ứng:
(1) C + H2O
→(2) H2S + O2 →
(3) CaOCl2 + HCl đặc →
(4) Al + dung dịch NaOH →
(5) F2 + H2O
→(6) Na2S2O3 + dung dịch H2SO4 →
Số phản ứng tạo ra đơn chất là:
- A. 4.
- B. 6.
- C. 3.
- D. 5.
/div>
Câu 40. Hỗn hợp X gồm anđehit Y, axit cacboxylic Z và este T (Z và T là đồng phân). Đốt cháy hoàn toàn 0,2 mol X cần 0,625mol O2, thu được 0,525 mol CO2 và 0,525 mol nước. Cho một lượng Y vừa bằng lượng Y có trong 0,2mol X tác dụng với một lượng dư dung dịch AgNO3 trong NH3, đun nóng, sau phản ứng được m gam Ag (hiệu suất phản ứng 100%). Giá trị của m là:
- A. 21,6.
- B. 16,2.
- C. 32,4.
- D. 64,8.
Xem thêm bài viết khác
- Thi THPTQG 2020: Đề thi và đáp án môn Hóa học mã đề 216
- HOT: Đề thi minh họa môn Hóa Học lần 3 của Bộ Giáo Dục
- Đáp án Đề thi thử THPT quốc gia môn Hóa năm 2017 của trường THPT chuyên ĐHSP
- Đề 4: Luyện thi THPTQG môn Hóa học năm 2019
- Lời giải câu số 20, 21, 33 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 13
- Cách làm câu số 13, 16, 38 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 30
- Thi THPTQG 2020: Đề thi và đáp án môn Hóa học mã đề 204
- Đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 30
- Cách làm câu số 19, 22, 23 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 24
- Đề và đáp án môn Hóa học mã đề 222 thi THPT quốc gia năm 2017 đáp án của bộ GD-ĐT
- Lời giải câu số 8, 11, 29 đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 1
- Đáp án Đề thi thử THPT quốc gia môn Hóa Học năm 2017 Đề số 17











