Giải bài 45 hóa 11: Axit cacboxylic sgk trang 205
Giải hóa học lớp 11 tập 2, giải bài 45 Axit cacboxylic trang 205 sgk hóa học 11, để học tốt hóa học 11. Bài này sẽ giúp các em nắm vững được lý thuyết cũng như cách giải các bài tập của bài Luyện tập. Cách làm đầy đủ, chi tiết và rõ ràng.
Nội dung bài viết gồm 2 phần:
- Ôn tập lý thuyết
- Hướng dẫn giải bài tập sgk
A. LÝ THUYẾT
I. Định nghĩa, phân loại, danh pháp
1. Định nghĩa
- Axit cac boxylic là những hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hidro.
2. Phân loại
- Axit no, đơn chức, mạch hở: Gốc ankyl+ nhóm –COOH: CTCT thu gọn của dãy đồng đẳng CnH2n+1COOH (n≥0) , CTPT chung CmH2mO2 (m≥1).
- Axit không no, đơn chức, mạch hở: Gốc hidrocacbon không no + nhóm –COOH.
- Axit thơm đơn chức: Gốc hidrocacbon thơm + nhóm –COOH.
- Axit đa chức: Axit có 2 hay nhiều nhóm –COOH.
3. Danh pháp
- Tên thay thế:
Axit + tên hidrocacbon no tương ứng với mạch chính + oic
II. Đặc điểm cấu tạo
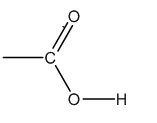
Nhóm cacboxyl có cấu tạo:
- Nhóm cacboxyl có cấu tạo: Nhóm C = O không giống trong anđehit và xeton.
- Nhóm – O – H phân cực hơn nhóm – O – H trong ancol và phenol.
- Tính axit lớn hơn ancol và phenol.
III. Tính chất vật lý
- Trạng thái: ở điều kiện thường, axit cacboxylic ở trạng thái lỏng hoặc rắn
- Nhiệt độ sôi: cao hơn anđehit, xeton và ancol tương ứng có cùng số C
- Tính tan: do có liên kết hidro với nước, các axit tan được trong nước.
- Axit có vị chua
IV. Tính chất hóa học
1. Tính axit
- Trong dung dịch, axit phân ly thuận nghịch
RCOOH ⥩ RCOO- + H+
- Tác dụng với bazơ, oxit bazơ tạo thành muối và nước
RCOOH + NaOH → RCOONa + H2O
2RCOOH + ZnO → (RCOO)2Zn + H2O
- Tác dụng với muối
2RCOOH + CaCO3→ (RCOO)2Ca + CO2 + H2O
- Tác dụng với kim loại hoạt trước hidro trong dãy hoạt động hóa học của các kim loại tạo thành muối và giải phóng khí hidro
2RCOOH + Zn → (RCOO)2Zn + H2
2. Phản ứng thế nhóm -OH
- Phản ứng este hóa
RCOOH + R’OH ⥩ RCOOR’ + H2O
V. Điều chế
1. Phương pháp lên men giấm
C2H5OH + O2→ CH3COOH + H2O(xt: men giấm)
2. Oxi hóa andehit
2RCHO + O2→ 2RCOOH
3. Oxi hóa ankan
2CH3CH2CH2CH3 + 5O2→ 4CH3COOH + 2H2O
R-CH2-CH2-R1 + O2→ R-COOH + R1-COOH +2H2O
4. Từ metanol
CH3OH + CO → CH3COOH
VI. Ứng dụng
- Làm nguyên liệu cho công nghiệp mĩ phẩm, công nghiệp dệt, công nghiệp hóa học…
Xem thêm bài viết khác
- Giải câu 4 bài 24: Luyện tập: Hợp chất hữu cơ. Công thức phân tử và công thức cấu tạo
- Giải câu 7 bài 31: Luyện tập : Anken và ankađien sgk Hóa học 11 trang 137
- Giải câu 7 bài 5 Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Giải câu 6 bài 3 Sự điện li của nước. pH. Chất chỉ thị axit bazơ
- Giải câu 3 bài 35 Benzen và đồng đẳng. Một số hidrocacbon thơm khác sgk Hóa học 11 trang 159
- Giải thí nghiệm 3 bài 14: Bài thực hành 2 -Tính chất của một số hợp chất nitơ
- Giải câu 1 bài 41 hóa 11: Phenol sgk trang 193
- Giải câu 1 bài 24: Luyện tập: Hợp chất hữu cơ. Công thức phân tử và công thức cấu tạo
- Giải câu 7 bài 22: Cấu trúc phân tử hợp chất hữu cơ
- Giải câu 6 bài 27: Luyện tập : Ankan và xicloankan sgk Hóa học 11 trang 122
- Giải câu 6 bài 21: Công thức phân tử hợp chất hữu cơ
- Giải bài 37 hoá 11: Nguồn hidrocacbon thiên nhiên sgk trang 163











