Giải bài 9: Axit nitric và muối nitrat
Bài học này trình bày nội dung: Axit nitric và muối nitrat . Dựa vào cấu trúc SGK hóa học lớp 9, KhoaHoc sẽ tóm tắt lại hệ thống lý thuyết và hướng dẫn giải các bài tập 1 cách chi tiết, dễ hiểu. Hi vọng rằng, đây sẽ là tài liệu hữu ích giúp các em học tập tốt hơn.
A - KIẾN THỨC TRỌNG TÂM
AXIT NITRIC
I. Cấu tạo phân tử và tính chất vật lí
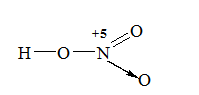
- Axit nitric là chất lỏng không màu, tan vô hạn trong nước.
II. Tính chất hoá học
1. Tính axit
HNO3 → H+ + NO3-
- Làm quỳ tím hoá đỏ
- Tác dụng với bazơ. VD: HNO3 + NaOH → NaNO3 + H2O
- Tác dụng với oxit bazơ. VD: 2HNO3 + MgO → Mg(NO3)2 + H2O
- Tác dụng với muối. VD: 2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
2. Tính oxi hoá
- Tác dụng với kim loại
- HNO3 tác dụng với hầu hết các kim loại (trừ Au, Pt) oxi hoá kim loại đến mức cao nhất, không giải phóng hiđro.
Cu + 4HNO3 (đặc) → Cu(NO3)2 + 2NO2 + 2H2O
Cu + 4H+ + 2NO3- →Cu2+ + 2NO2 + 2H2O
- Kim loại tác dụng với HNO3 đặc nóng thì luôn giải phóng NO2
- Nếu HNO3 loãng thì tạo thành N2, NO, N2O, NH4NO3.
- HNO3 đặc nguội thụ động với nhôm, sắt, crôm.
- Tác dụng với phi kim: HNO3 đặc có thể oxi hóa được S, P, C ... trong điều kiện đun nóng. Ví dụ:
![]()
- Tác dụng với hợp chất
3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O
III. Ứng dụng
- Phần lớn axit nitric sản suất được dùng để điều chế phân đạm. Ngoài ra còn được dùng sản xuất thuốc nổ.
IV. Điều chế
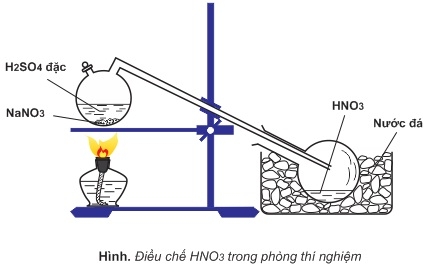
1. Trong phòng thí nghiệm
NaNO3 + H2SO4 → NaHSO4 + HNO3
2. Trong công nghiệp
Axit nitric được sản xuất qua ba giai đoạn
- Oxi hoá NH3
![]()
- Oxi hoá NO:NO + O2 → 2NO2
- Hợp nước tạo thành HNO3 : 4NO2 +O2 + 2H2O → HNO3
MUỐI NITRAT
I. Tính chất của muối nitrat
1. Tính chất vật lí
- Tất cả các muối nitrat đều là chất rắn, dễ tan trong nước và là điện li mạnh.
2. Phản ứng nhiệt phân
![]()
![]()
II. Ứng dụng
- Các muối nitrat chủ yếu được sử dụng làm phân bón ngoài ra nó còn được làm thuốc nổ.
B. BÀI TẬP VÀ HƯỚNG DẪN GIẢI
Kiến thức thú vị
Câu 1.(Trang 45 /SGK)
Viết công thức electron, công thức cấu tạo của axit nitric. Cho biết nguyên tố nitơ có hóa trị và số oxi hóa bao nhiêu ?
Câu 2.(Trang 45 /SGK)
Lập các phương trình hóa học:
a) Ag + HNO3 (đặc) → NO2 + ? + ?
b) Ag + HNO3 (loãng) → NO + ? + ?
c) Al + HNO3 → N2O + ? + ?
d) Zn + HNO3 → NH4NO3 + ? + ?
e) FeO + HNO3 → NO + Fe(NO3)3 + ?
g) Fe3O4 + HNO3 → NO + Fe(NO3)3 + ?
Câu 3.(Trang 45 /SGK)
Hãy chỉ ra những tính chất hóa học chung và khác biệt giữa axit nitric và axit sunfuric. Viết các phương trình hóa học để minh họa.
Câu 4.(Trang 45 /SGK)
a) Trong phương trình hóa học của phản ứng nhiệt phân sắt (III) nitrat, tổng các hệ số bằng bao nhiêu ?
A. 5 B. 7 C. 9 D. 21
b) Trong phương trình hóa học của phản ứng nhiệt phân thủy ngân (II) nitrat, tổng các hệ số bằng bao nhiêu ?
A. 5 B. 7 C. 9 D. 21
Câu 5.(Trang 45/SGK)
Viết phương trình hóa học của các phản ứng thực hiện dãy chuyển hóa sau đây:

Câu 6.(Trang 45 /SGK)
Khi hòa tan 30,0 g hỗn hợp đồng và đồng (II) oxit trong 1,50 lít dung dịch axit nitric 1,00 M (loãng) thấy thoát ra 6,72 lít nitơ monoaxit (đktc). Xác định hàm lượng phần trăm của đồng (II) oxit trong hỗn hợp, nồng độ mol của đồng (II) nitrat và axit nitric trong dung dịch sau phản ứng, biết rằng thể tích dung dịch không thay đổi.
Câu 7.(Trang 45 /SGK)
Để điều chế 5,000 tấn axit nitric nồng độ 60,0 % cần dùng bao nhiêu tấn amoniac ? Biết rằng sự hao hụt amoniac trong quá trình sản xuẩ là 3,8 %.











