Đề 1: Luyện thi THPTQG môn Hóa học năm 2019
Đề 1: Luyện thi THPTQG môn Hóa học năm 2019. Đề gồm 40 câu hỏi, các em học sinh làm trong thời gian 50 phút. Khi làm xong, các em sẽ biết số điểm của mình và đáp án các câu hỏi. Hãy nhấn chữ bắt đầu ở phía dưới.
Câu 1: Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy muối halogen?
- A. Fe.
- B. Al.
- C. Cu.
- D. Na.
Câu 2: Số nguyên tử oxi trong một phân tử chất béo là
- A. 6.
- B. 2.
- C. 4.
- D. 8.
Câu 3: Natri clorua có nhiều trong nước biển, là thành phần chính của muối ăn. Công thức của natriclorua là
- A. NaCl.
- B. CaCl2.
- C. NaI.
- D. KBr.
Câu 4: Etyl fomat là este có mùi thơm, không độc, được dùng làm chất tạo hương trong công nghiệp thực phẩm. Công thức của etyl fomat là
- A.

- B.

- C.

- D.

Câu 5: Ion kim loại nào sau đây có tính oxi hóa mạnh nhất ?
- A. Ag+
- B. Al3+
- C. Fe2+
- D. Cu2+
Câu 6: Cho lượng dư dung dịch NaOH vào dung dịch nào sau đây không thu được kết tủa?
- A.
 .
. - B.
 .
. - C.
 .
. - D.
 .
.
Câu 7: Chất nào sau đây thuộc loại đisaccarit?
- A. Saccarozơ.
- B. Glucozơ.
- C. Tinh bột.
- D. Xenlulozơ.
Câu 8: Amin và amino axit đều tác dụng với dung dịch nào sau đây?
- A. NaCl.
- B.
 .
. - C. HCl.
- D. NaOH.
Câu 9: Bảo quản thực phẩm (thịt, cá...) theo phương nào sau đây được coi là an toàn?
- A. Dùng phân đạm, nước đá.
- B. Dùng nước đá và nước đá khô.
- C. Dùng fomon, nước đá.
- D. Dùng nước đá khô, fomon.
Câu 10: Chất nào sau đây tác dụng với ![]() được dung dịch màu tím
được dung dịch màu tím
- A. Gly-Ala.
- B. Glyxerol.
- C. Gly-Ala-Val.
- D. Anilin.
Câu 11: Kim loại nào sau đây được dùng chế tạo tế bào quang điện?
- A. K.
- B. Cs.
- C. Na.
- D. Al.
Câu 12: Polime X chỉ chứa hai nguyên tố cacbon và hiđro, được dùng để làm màng mỏng, bình chứa, túi đựng. Tên của X là
- A. polietilen.
- B. polibutađien.
- C. poli(vinyl clorua).
- D. poliacrilonitrin.
Câu 13: Thủy phân hoàn toàn este X (trong môi trường axit) thu được hai sản phẩm đều tham gia phản ứng tráng bạc. Công thức phân tử phù hợp với X có thể là
- A.
 .
. - B.
 .
. - C.
 .
. - D.
 .
.
Câu 14: Cho các sơ đồ sau:
![]() + HCl→ $X_{1}$; $X_{1}$ + NaOH dư → $X_{2}$;
+ HCl→ $X_{1}$; $X_{1}$ + NaOH dư → $X_{2}$;
![]() + NaOH → $Y_{1}$; $Y_{1}$ + HCl dư → $Y_{2}$.
+ NaOH → $Y_{1}$; $Y_{1}$ + HCl dư → $Y_{2}$.
Kết luận nào sau đây là đúng?
- A.
 khác $Y_{2}$.
khác $Y_{2}$. - B.
 , $X_{2}$, $Y_{1}$, $Y_{2}$ là 4 chất khác nhau.
, $X_{2}$, $Y_{1}$, $Y_{2}$ là 4 chất khác nhau. - C.
 khác $Y_{1}$.
khác $Y_{1}$. - D.
 trùng với $Y_{2}$, $X_{2}$ trùng với $Y_{1}$.
trùng với $Y_{2}$, $X_{2}$ trùng với $Y_{1}$.
Câu 15: Cho hỗn hợp gồm K, Na, Ba tác dụng hết với nước được dung dịch X và 4,48 lít khí (đktc). Để trung hòa X cần vừa đủ V lít dung dịch ![]() 0,5 M. Giá trị của V là
0,5 M. Giá trị của V là
- A. 0,8 lít.
- B. 0,2 lít.
- C. 0,4 lít.
- D. 0,6 lít.
Câu 16: Dãy các vật liệu được chế tạo từ polime trùng ngưng là
- A. nilon-6; nilon-6,6; nhựa novolac.
- B. tơ visco; nilon-6,6; cao su buna-N.
- C. thủy tinh plexiglat; nhựa rezol; nhựa PVC.
- D. cao su buna-S; tơ olon; nilon-6.
Câu 17: Phát biểu nào sau đây đúng?
- A. Axetilen khử được Ag+ trong dung dịch
 .
. - B. Metanol, Etanol tan vô hạn trong nước ở điều kiện thường.
- C. Etilen bị H2 (Ni, t°) khử thành etan.
- D. Các axit cacboxylic đều tan tốt trong nước.
Câu 18: Đun nóng 6 gam axit axetic với 6 gam ancol etylic có ![]() đặc làm xúc tác. Khối lượng este tạo thành khi hiệu suất phản ứng đạt 80% là
đặc làm xúc tác. Khối lượng este tạo thành khi hiệu suất phản ứng đạt 80% là
- A. 8,00 gam.
- B. 12,00 gam.
- C. 10,00 gam.
- D. 7,04 gam.
Câu 19: Saccarozơ và glucozơ đều có
- A. phản ứng với dung dịch NaCl.
- B. phản ứng với
 ở điều kiện thường tạo dung dịch màu xanh lam.
ở điều kiện thường tạo dung dịch màu xanh lam. - C. phản ứng với dung dịch
 trong $NH_{3}$.
trong $NH_{3}$. - D. phản ứng thủy phân trong môi trường axit.
Câu 20: Cho từ từ 400 ml dung dịch HCl 0,5M đến hết vào bình đựng 100ml dung dịch chứa đồng thời ![]() 1,5M và $NaHCO_{3}$ 1M, kết thúc thí nghiệm được V lít khí (đktc).Giá trị của V là
1,5M và $NaHCO_{3}$ 1M, kết thúc thí nghiệm được V lít khí (đktc).Giá trị của V là
- A. 2,24 lít.
- B. 3,36 lít.
- C. 4,48 lít.
- D. 1,12 lít.
Câu 21: Cho 0,15 mol axit glutamic vào 175 ml dung dịch HCl 2M, thu được dung dịch X. Cho dung dịch NaOH dư vào X. Sau khi phản ứng xảy ra hoàn toàn, số mol NaOH tham gia phản ứng là
- A. 0,35 mol.
- B. 0,50 mol.
- C. 0,65 mol.
- D. 0,55 mol.
Câu 22: Phát biểu nào sau đây sai?
- A. Các chất béo thường không tan trong nước và nhẹ hơn nước.
- B. Chất béo là trieste của Glixerol với các axit đơn chức.
- C. Triolein có khả năng tham gia phản ứng cộng hiđro khi đun nóng có xúc tác Ni.
- D. Chất béo bị thủy phân khi đun nóng trong dung dịch kiềm.
Câu 23: Cho hỗn hợp gồm Fe và Mg vào dung dịch ![]() đến khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X là
đến khi các phản ứng xảy ra hoàn toàn thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X là
- A.
 và $AgNO_{3}$.
và $AgNO_{3}$. - B.
 và $Mg(NO_{3})_{2}$.
và $Mg(NO_{3})_{2}$. - C.
 và $Mg(NO_{3})_{2}$.
và $Mg(NO_{3})_{2}$. - D.
 và $Fe(NO_{3})_{2}$.
và $Fe(NO_{3})_{2}$.
Câu 24: Phản ứng hóa học nào sau đây có phương trình ion thu gọn là: ![]() ?
?
- A.
 .
. - B.
 .
. - C.
 .
. - D.
 .
.
Câu 25: Hỗn hợp X gồm ![]() , $C_{2}H_{4}$ và $C_{3}H_{6}$ có tỉ khối so với
, $C_{2}H_{4}$ và $C_{3}H_{6}$ có tỉ khối so với ![]() là 9,25. Cho 22,4 lít X (đktc) vào bình kín có sẵn một ít bột Ni. Đun nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với
là 9,25. Cho 22,4 lít X (đktc) vào bình kín có sẵn một ít bột Ni. Đun nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với ![]() bằng 10. Tổng số mol
bằng 10. Tổng số mol ![]() đã phản ứng làP
đã phản ứng làP
- A. 0,050 mol.
- B. 0,075 mol.
- C. 0,015 mol.
- D. 0,070 mol.
Câu 26: Cho các phát biểu sau:
(a). Các polime thiên nhiên đều có ít nhất 3 nguyên tố C, H, O.
(b). Ở điều kiện thích hợp, triolein tham gia phản ứng cộng ![]() .
.
(c). Tinh bột và xenlulozơ là đồng phân của nhau.
(d). Muối phenylamoni clorua tan được trong nước.
(e). Trong phân tử peptit mạch hở Gly-Ala-Glu có 4 nguyên tử oxi.
(g). Ở nhiệt độ thường, glixerol hòa tan được ![]() .
.
Số phát biểu đúng là
- A. 4.
- B. 2.
- C. 3.
- D. 5.
Câu 27: Nhỏ từ từ dung dịch ![]() đến dư vào dung dịch hỗn hợp $Na_{2}SO_{4}$ và $Al_{2}(SO_{4})_{3}$ ta có đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo số mol
đến dư vào dung dịch hỗn hợp $Na_{2}SO_{4}$ và $Al_{2}(SO_{4})_{3}$ ta có đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo số mol ![]() như sau:
như sau:

Giá trị của m theo đồ thị là:
- A. 73,02.
- B. 82,38.
- C. 79,26.
- D. 77,70.
Câu 28: Hoà tan hoàn toàn 14,4 gam hỗn hợp Fe, Cu (tỉ lệ mol 1 : 1) bằng axit ![]() , thu được V lít (đktc) hỗn hợp khí X (gồm NO và $NO_{2}$) và dung dịch Y (chứa hai muối và axit dư). Tỉ khối của X đối với $H_{2}$ bằng 19. Giá trị của V là:
, thu được V lít (đktc) hỗn hợp khí X (gồm NO và $NO_{2}$) và dung dịch Y (chứa hai muối và axit dư). Tỉ khối của X đối với $H_{2}$ bằng 19. Giá trị của V là:
- A. 6,72.
- B. 4,48.
- C. 2,24.
- D. 5,60.
Câu 29: Hợp chất X là este đơn chức, mạch hở. Đốt cháy hoàn toàn a mol X cần vừa đủ V lít ![]() (đktc), tạo ra b mol $CO_{2}$ và d mol $H_{2}O$. Biết a = b – d và V = 100,8a. Số đồng phân cấu tạo của X thỏa mãn là
(đktc), tạo ra b mol $CO_{2}$ và d mol $H_{2}O$. Biết a = b – d và V = 100,8a. Số đồng phân cấu tạo của X thỏa mãn là
- A. 4.
- B. 5.
- C. 3.
- D. 6.
Câu 30: Thực hiện các thí nghiệm sau:
(a) Cho dung dịch NaOH đến dư vào dung dịch ![]() .
.
(b) Cho dung dịch ![]() vào dung dịch $FeCl_{3}$.
vào dung dịch $FeCl_{3}$.
(c) Sục khí ![]() đến dư vào dung dịch $Ca(OH)_{2}$.
đến dư vào dung dịch $Ca(OH)_{2}$.
(d) Cho dung dịch NaOH vào dung dịch ![]() .
.
(e) Cho dung dịch ![]() vào dung dịch $BaCl_{2}$.
vào dung dịch $BaCl_{2}$.
(g) Sục khí ![]() dư vào dung dịch $NaAlO_{2}$.
dư vào dung dịch $NaAlO_{2}$.
Sau khi các phản ứng xảy ra, số thí nghiệm thu được kết tủa là
- A. 4.
- B. 5.
- C. 6.
- D. 3.
Câu 31: Cho các phát biểu sau:
(a) Cho mẩu Na vào dung dịch ![]() có khí thoát ra và dung dịch xuất hiện kết tủa xanh lam.
có khí thoát ra và dung dịch xuất hiện kết tủa xanh lam.
(b) Tính chất vật lí chung của kim loại là: Tính dẫn điện, dẫn nhiệt, ánh kim và tính cứng.
(c) Nước cứng vĩnh cửu là nước cứng có chứa ![]() và $Cl^{-}$.
và $Cl^{-}$.
(d) Thạch cao sống dùng để sản xuất xi măng.
(e) Tinh thể ![]() được dùng làm đồ trang sức, chế tạo chân kính đồng hồ...
được dùng làm đồ trang sức, chế tạo chân kính đồng hồ...
(g) ![]() bị khử bởi $Ag^{+}$ thành Ag và $Fe^{3+}$.
bị khử bởi $Ag^{+}$ thành Ag và $Fe^{3+}$.
Số phát biểu đúng là
- A. 2.
- B. 4.
- C. 3.
- D. 5.
Câu 32: Tiến hành các thí nghiệm sau:
(a) Nhúng thanh Fe nguyên chất vào dung dịch ![]() .
.
(b) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm.
(c) Nhúng thanh Zn vào dung dịch HCl có lẫn một ít ![]() .
.
(d) Nhúng thanh Cu nguyên chất vào dung dịch ![]() .
.
(e) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào dung dịch ![]() loãng.
loãng.
Trong các thí nghiệm trên, số thí nghiệm xảy ra ăn mòn điện hóa học là
- A. 4.
- B. 2.
- C. 5.
- D. 3.
Câu 33: Hòa tan hoàn toàn m gam hỗn hợp X gồm K, ![]() , Na, $Na_{2}O$, Ba và BaO (trong đó oxi chiếm 10% về khối lượng) vào nước, thu được 300 ml dung dịch Y và 0,336 lít khí $H_{2}$ (đktc). Trộn 300 ml dung dịch Y với 200 ml dung dịch gồm HCl 0,2M và $HNO_{3}$ 0,15M được 500 ml dung dịch có pH = 2. Giá trị của m là
, Na, $Na_{2}O$, Ba và BaO (trong đó oxi chiếm 10% về khối lượng) vào nước, thu được 300 ml dung dịch Y và 0,336 lít khí $H_{2}$ (đktc). Trộn 300 ml dung dịch Y với 200 ml dung dịch gồm HCl 0,2M và $HNO_{3}$ 0,15M được 500 ml dung dịch có pH = 2. Giá trị của m là
- A. 2,8.
- B. 5,6.
- C. 5,2.
- D. 1,2.
Câu 34: Tiến hành điện phân V lít dung dịch chứa ![]() 1M và NaCl 0,5M (điện cực trơ) đến khi khối lượng dung dịch giảm m gam thì dừng điện phân. Cho 9,5 gam Fe vào dung dịch sau điện phân, kết thúc phản ứng thu được 1,12 lít khí NO thoát ra (sản phẩm khử duy nhất) và còn lại 5,7 gam hỗn hợp rắn không tan. Giá trị của m gần nhất với giá trị nào sau đây?
1M và NaCl 0,5M (điện cực trơ) đến khi khối lượng dung dịch giảm m gam thì dừng điện phân. Cho 9,5 gam Fe vào dung dịch sau điện phân, kết thúc phản ứng thu được 1,12 lít khí NO thoát ra (sản phẩm khử duy nhất) và còn lại 5,7 gam hỗn hợp rắn không tan. Giá trị của m gần nhất với giá trị nào sau đây?
- A. 12,8.
- B. 14,7.
- C. 15,4.
- D. 17,6.
Câu 35: Hỗn hợp X gồm các peptit mạch hở (tạo từ Ala, Gly, Val) và chất béo Y (tạo từ một axit béo no). Đốt cháy hoàn toàn X thu được 0,722 mol ![]() . Mặt khác, để thủy phân hoàn toàn X cần dùng vừa đủ 0,056 mol NaOH thu được muối Z và glixerol. Đốt cháy hoàn toàn Z thu được $Na_{2}CO_{3}$, 0,684 mol $CO_{2}$ và 0,694 mol
. Mặt khác, để thủy phân hoàn toàn X cần dùng vừa đủ 0,056 mol NaOH thu được muối Z và glixerol. Đốt cháy hoàn toàn Z thu được $Na_{2}CO_{3}$, 0,684 mol $CO_{2}$ và 0,694 mol ![]() . Phần % khối lượng của Y trong X gần nhất với giá trị nào sau đây?
. Phần % khối lượng của Y trong X gần nhất với giá trị nào sau đây?
- A. 79.
- B. 85.
- C. 91.
- D. 87.
Câu 36: Cho m gam hỗn hợp X chứa Al, ![]() và 0,1 mol $Fe_{3}O_{4}$ tan hết trong dung dịch chứa 1,025 mol $H_{2}SO_{4}$. Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hóa nâu ngoài không khí và dung dịch Z chỉ chứa các muối sunfat trung hòa có khối lượng là 132,5 gam. Biết tỷ khối của Y so với $H_{2}$ là 31/3. Cho một lượng vừa đủ $BaCl_{2}$ vào Z sau khi các phản ứng xảy ra xong cho tiếp $AgNO_{3}$ dư vào thì thu được x gam kết tủa. Biết các phản ứng hoàn toàn. Giá trị của tổng x + m là
và 0,1 mol $Fe_{3}O_{4}$ tan hết trong dung dịch chứa 1,025 mol $H_{2}SO_{4}$. Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hóa nâu ngoài không khí và dung dịch Z chỉ chứa các muối sunfat trung hòa có khối lượng là 132,5 gam. Biết tỷ khối của Y so với $H_{2}$ là 31/3. Cho một lượng vừa đủ $BaCl_{2}$ vào Z sau khi các phản ứng xảy ra xong cho tiếp $AgNO_{3}$ dư vào thì thu được x gam kết tủa. Biết các phản ứng hoàn toàn. Giá trị của tổng x + m là
- A. 334,025.
- B. 533,000.
- C. 628,200.
- D. 389,175.
Câu 37: Để phân tích định tính các nguyên tố trong hợp chất hữu cơ, người ta thực hiện một thí nghiệm được mô tả như hình vẽ:
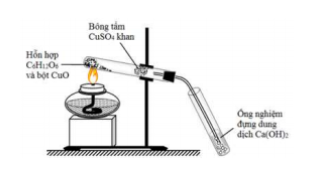
Cho các phát biểu sau:
(a) Bông trộn ![]() khan luôn chuyển thành màu xanh.
khan luôn chuyển thành màu xanh.
(b) Bình đựng dung dịch ![]() luôn thu được kết tủa.
luôn thu được kết tủa.
(c) Thí nghiệm trên dùng để xác định nitơ có trong hợp chất hữu cơ.
(d) Trong thí nghiệm trên có thể thay dung dịch ![]() bằng dung dịch $Ba(OH)_{2}$.
bằng dung dịch $Ba(OH)_{2}$.
(e) Bông trộn CuSO4 khan có tác dụng chính là ngăn hơi hợp chất hữu cơ thoát ra khỏi ống nghiệm.
Số phát biểu đúng là
- A. 4.
- B. 2.
- C. 3.
- D. 1.
Câu 38: Có 2 dung dịch X,Y loãng, mỗi dung dịch chứa một chất tan và có số mol bằng nhau. Tiến hành các thí nghiệm sau:
- Thí nghiệm 1: Cho bột Fe dư vào dung dịch X được n1 mol một chất khí duy nhất không màu, hóa nâu ngoài không khí.
- Thí nghiệm 2: Cho bột Fe dư dung dịch Y được n2 mol một chất khí duy nhất không màu không hóa nâu ngoài không khí.
- Thí nghiệm 3: Trộn dung dịch X với dung dịch Y rồi thêm bột Fe đến dư được n3 mol một chất khí duy nhất không màu, hóa nâu ngoài không khí. Biết các phản ứng xảy ra hoàn toàn, chỉ tạo muối của kim loại và n2 = n3 = 2n1. Hai dung dịch X, Y lần lượt là
- A.
 , $H_{2}SO_{4}$.
, $H_{2}SO_{4}$. - B.
 , $H_{2}SO_{4}$.
, $H_{2}SO_{4}$. - C.
 , $NaHSO_{4}$.
, $NaHSO_{4}$. - D.
 , $NaHCO_{3}$.
, $NaHCO_{3}$.
Câu 39: Cho hỗn hợp E gồm một axit X (no, đơn chức, mạch hở) và một este Y(hai chức, mạch hở, không no có 1 liên kết C=C) tác dụng vừa đủ với 110 ml dung dịch KOH 1M, thu được hỗn hợp muối Z và hơi một ancol no, đơn chức (ở đktc). Dẫn lượng ancol trên vào bình chứa Na dư thấy thoát ra 896 ml H2 ở đktc và bình tăng 2,48 gam. Đốt cháy hoàn toàn Z thu được ![]() và 10,65 gam hỗn hợp $CO_{2}$ và $H_{2}O$. Phần trăm khối lượng của Y có trong E là:
và 10,65 gam hỗn hợp $CO_{2}$ và $H_{2}O$. Phần trăm khối lượng của Y có trong E là:
- A. 69,44%.
- B. 70,21%.
- C. 71,02%.
- D. 72,18%.
Câu 40: X chứa một amin no đơn chức (biết trong X có số C lớn hơn 2), mạch hở . Y chứa hai α- amino axit đồng đẳng kế tiếp thuộc dãy đồng đẳng của glyxin. Đốt cháy hết 0,47 mol hỗn hợp Z chứa X, Y bằng lượng oxi vừa đủ, thu được 60,72 gam ![]() . Biết Z tác dụng vừa đủ với 70 ml NaOH 1M. Phần % khối lượng của α-amino axit có khối lượng phân tử lớn hơn gần nhất với giá trị nào sau đây
. Biết Z tác dụng vừa đủ với 70 ml NaOH 1M. Phần % khối lượng của α-amino axit có khối lượng phân tử lớn hơn gần nhất với giá trị nào sau đây
- A. 48.
- B. 8.
- C. 80.
- D. 12.











