Giải bài 22: Cấu trúc phân tử hợp chất hữu cơ
Dựa theo cấu trúc SGK hóa học 11, Tech 12h xin chia sẻ với các bạn bài: Cấu trúc phân tử hợp chất hữu cơ. Với kiến thức trọng tâm và các bài tập có lời giải chi tiết, hi vọng rằng đây sẽ là tài liệu giúp các bạn học tập tốt hơn.
A – KIẾN THỨC TRỌNG TÂM
I. Công thức cấu tạo
- Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết ( liên kết đơn, liên kết bội) của các nguyên tử trong phân tử.
- Các loại công thức cấu tạo

II. Thuyết cấu tạo hoá học
- Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hóa trị và theo một thứ tự nhất định. Thứ tự liên kết đó gọi là cấu tạo hóa học. Sự thay đổi thứ tự liên kết đó, tức là thay đổi cấu tạo hóa học, sẽ ra hợp chất khác.
- Trong phân tử hợp chất hữu cơ, cacbon có hóa trị bốn. Nguyên tử các bon không những có thể liên kết với nguyên tử của nguyên tố khác mà còn liên kết với nhau tạo thành mạch cacbon ( mạch vòng, mạch không vòng, mạch nhánh, mạch không nhánh).
- Tính chất của các chất phụ thuộc vào thành phần phân tử ( bản chất, số lượng các nguyên tử) và cấu tạo hóa học ( thứ tự liên kết các nguyên tử).
III. Đồng đẳng, đồng phân
1. Đồng đẳng
- Khái niệm: Những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hoá học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
- Ví dụ: C2H4, C3H6, C4H8,… CnH2n
2. Đồng phân
- Khái niệm: Những hợp chất khác nhau nhưng có cùng công thức phân tử là những chất đồng phân.
- Phân loại: đồng phân lập thể và đồng phân cấu tạo.
- Ví dụ: Ancol etylic (CH3 – CH2 – OH) và đimetyl ete (CH3 – O – CH3)
IV. Liên kết trong phân tử hợp chất hữu cơ
- Liên kết đơn (liên kết δ) do một cặp electron dùng chung tạo nên và được biểu diễn bằng một gạch nối giữa hai nguyên tử. Liên kết δ là liên kết bền
- Liên kết đôi do 2 cặp eletron chung giữa hai nguyên tử tạo nên. Liên kết đôi gồm một liên kết δ và một liên kết π.
- Liên kết ba do 3 cặp electron chung giữa hai nguyên tử tạo nên. Liên kết ba gồm một liên kết δ và hai liên kết π.
B. BÀI TẬP VÀ HƯỚNG DẪN GIẢI
Kiến thức thú vị
Câu 1. (Trang 101 SGK)
Phát biểu nội dung cơ bản của thuyết cấu tạo hoá học.
Câu 2. (Trang 101 /SGK)
So sánh ý nghĩa của công thức phân tử và công thức cấu tạo. Cho thí dụ minh hoạ.
Câu 3. (Trang 101 /SGK)
Thế nào là liên kết đơn, liên kết đôi, liên kết ba ?
Câu 4. (Trang 101 /SGK)
Chất nào sau đây trong phân tử chỉ có liên kết đơn ?
A. CH4
B. C2H4
C. C6H6
D. CH3COOH
Câu 5. (Trang 101 SGK)
Những chất nào sau đây là đồng đẳng của nhau, đồng phân của nhau ?
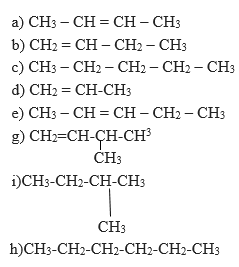
Câu 6. (Trang 102 SGK) Viết công thức cấu tạo có thể có của các chất có công thức phân tử như sau: C2H6O, C3H6O, C4H10.
Câu 7. (Trang 102 SGK) Những công thức cấu tạo nào dưới đây biểu thị cùng một chất ?
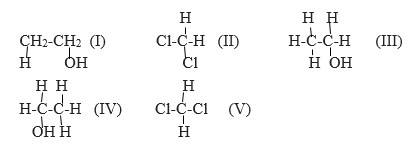
Câu 8. (Trang 102 SGK) Khi cho 5,30 gam hỗn hợp gồm etanol C2H5OH và propan-1-ol CH3CH2CH2OH tác dụng với natri (dư) thu được 1,12 lít khí (đktc).
a) Viết phương trình hoá học của các phản ứng xảy ra.
b) Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp.
=> Trắc nghiệm hóa học 11 bài 22: Cấu trúc phân tử hợp chất hữu cơ
Xem thêm bài viết khác
- Giải câu 4 bài 22: Cấu trúc phân tử hợp chất hữu cơ
- Giải câu 3 bài 32 Ankin sgk Hóa học 11 trang 145
- Giải câu 4 bài 29: Anken sgk Hóa học 11 trang 132
- Cho 100 g khí oxi và 100 g khí cacbon đioxit, cả 2 khí đều ở 200C và 1 atm. Biết rằng thể tích mol khí ở những điều kiện này là 24 l.
- Giải câu 5 bài 13: Luyện tập tính chất của nitơ, photpho và các hợp chất của chúng
- Giải câu 6 bài 35 Benzen và đồng đẳng. Một số hidrocacbon thơm khác sgk Hóa học 11 trang 160
- Giải bài 47 hóa 11: Bài thực hành số 6: Tính chất của andehit và axit cacboxylic sgk trang 214
- Giải câu 5 bài 10: Photpho
- Giải câu 5 bài 30: Ankađien sgk Hóa học 11 trang 136
- Giải câu 2 bài 37 hoá 11: Nguồn hidrocacbon thiên nhiên sgk trang 169
- Giải câu 4 bài 18: Công nghiệp silicat
- Giải câu 4 bài 25: Ankan sgk Hóa học 11 trang 115











