Khoa học tự nhiên 8 bài 3 KHTN 8 bài 3: Oxi - Không khí
Khoa học tự nhiên 8 bài 3 được KhoaHoc đăng tải trong bài viết dưới đây nhằm giúp học sinh hoàn thiện đáp án cho các câu hỏi đồng thời nâng cao kết quả học tập môn KHTN lớp 8.
Soạn bài 3 KHTN 8
Tại sao các nhà leo núi hoặc những người thợ lặn phải đeo các bình dưỡng khí hoặc các thiết bị đặc biệt?
Tại sao động vật sống dưới nước dễ gặp phải tình trạng thiếu oxi hơn động vật sống trên cạn?
Lời giải
Các nhà leo núi, các thợ lặn phải đeo bình dưỡng khí hoặc các thiết bị đặc biệt vì khi họ leo núi hoặc lặn xuống biển thì ở đó là các môi trường có lượng oxi nhỏ.
Động vật sống dưới nước dễ gặp phải tình trạng thiếu oxi hơn vì ở dưới nước có ít oxi hơn trên cạn (oxi hòa tan ít trong nước).
B. Hoạt động hình thành kiến thức
1. Tính chất vật lí của oxi
Đọc thông tin và điền vào bảng.
Thông tin: Sgk trang 15
Tính chất vật lí:
|
2. Tính chất hóa học của oxi
a) Oxi tác dụng với kim loại và phi kim
Thí nghiệm 1:
Nêu hiện tượng quan sát được. So sánh mức độ cháy của lưu huỳnh trong không khí và của lưu huỳnh trong oxi.
Viết PTHH của phản ứng xảy ra trong thí nghiệm trên, biết rằng khi lưu huỳnh (S) cháy trong oxi (![]() ) tạo thành khí lưu huỳnh didoxxit
) tạo thành khí lưu huỳnh didoxxit ![]() (còn gọi là khí sunfuro) và rất ít lưu huỳnh trioxit.
(còn gọi là khí sunfuro) và rất ít lưu huỳnh trioxit.
Thí nghiệm 2:
Nêu hiện tượng quan sát được. So sánh mức độ cháy của photpho trong không khí và mức độ cháy của photpho trong oxi.
Viết PTHH của phản ứng xảy ra trong thí nghiệm trên (chú ý điều kiện của phản ứng), biết khi đốt photpho trong oxi tạo thành điphotpho pentaoxit ![]() (ở dạng bột trắng, tan được trong nước).
(ở dạng bột trắng, tan được trong nước).
Thí nghiệm 3:
Nêu hiện tượng quan sát được trong quá trình thí nghiệm.
Viết PTHH của phản ứng xảy ra trong thí nghiệm trên, biết khi đốt cháy sắt trong oxi, tạo ra các hạt nhỏ nóng chảy màu nâu là sắt (II, III) oxit, công thức hóa học là ![]() thường được gọi là oxit sắt từ.
thường được gọi là oxit sắt từ.
b) Oxi có tác dụng được với hợp chất không?
Viết phương trình phản ứng giữa metan với oxi
![]()
2. Hãy chọn từ/ cụm từ thích hợp cho dưới đấy để điền vào chỗ trống trong kết luận sau về tính chất hóa học của oxi.
(1) kim loại rất hoạt động; phim kim hoạt động bình thường; phi kim rất hoạt động.
(2) ở nhiệt độ cao; ở nhiệt độ thường; ở nhiệt độ thấp.
(3) lưu huỳnh; đồng; photpho; sắt; metan, ![]() ; cacbon; propan,
; cacbon; propan, ![]() ; butan,
; butan, ![]() .
.
(4) I; II; III.
Kết luận:
Khí oxi là một đơn chất ![]() , đặc biệt khi
, đặc biệt khi ![]() , dễ dàng tham gia phản ứng hóa học với nhiều phi kim (như
, dễ dàng tham gia phản ứng hóa học với nhiều phi kim (như ![]() ), nhiều kim loại (như
), nhiều kim loại (như ![]() ) và hợp chất (như
) và hợp chất (như ![]() ). Trong các hợp chất hóa học, nguyên tố oxi có hóa trị
). Trong các hợp chất hóa học, nguyên tố oxi có hóa trị ![]()
II. Sự oxi hóa. Phản ứng hóa hợp
1. Sự oxi hóa
Vậy sự oxi hóa một chất là gì? Điền từ/ cụm từ thích hợp cho trong ngoặc đơn để hoàn thành định nghĩa về sự oxi hóa.
(một chất, hai chất, nhiều chất, đơn chất, hợp chất)
Sự oxi hóa là sự tác dụng của oxi với ![]() (chất đó có thể là ...(2).... hoặc ...(3)...)
(chất đó có thể là ...(2).... hoặc ...(3)...)
2. Phản ứng hóa hợp
Hãy nhận xét, ghi số chất phản ứng và số chất chất sản phẩm trong các phản ứng hóa học sau đây và trả lời câu hỏi:
| Phản ứng hóa học | Số chất phản ứng | Số chất sản phẩm |
| (1) | 2 | 1 |
| (2) | ||
| (3) | ||
| (4) |
So sánh điểm giống và khác nhau về số chất tham gia phản ứng và số chất sản phẩm trong các phản ứng hóa học trên.
Chọn từ hoặc cụm từ cho dưới đây để hoàn thành định nghĩa phản ứng hóa hợp:
(1) Một chất mới, hai chất mới.
(2) một ban đầu; hai chất ban đầu; hai hay nhiều chất ban đầu.
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có ![]() được tạo thành từ $...(2)....$
được tạo thành từ $...(2)....$
III. Ứng dụng của oxi
Khí oxi có ứng dụng gì trong cuộc sống?
Quá trình hô hấp của sinh vật là quá trình lấy oxi và thải khí cacbonic. Khí oxi được cơ thể lấy vào và sử dụng như thế nào trong cơ thể thực vật và cơ thể người?
Hô hấp là quá trình vô cùng quan trọng đối với cơ thể con người. Nếu hệ hô hấp bị tổn thương thì cơ thể sẽ suy yếu rất nhanh và nếu không thở được, chỉ sau vài phút đã tử vong. Vậy chúng ta phải làm gì để giữ gìn và bảo vệ hô hấp?
Khí oxi có vai trò gì trong sự cháy?
Sự đốt cháy nhiên liệu là quá trình các nhiên liệu phản ứng với oxi và tỏa nhiều nhiệt. Hãy kể tên các ứng dụng sử dụng quá trình đốt cháy nhiên liệu này trong đời sống.
Tại sao nói sử dụng nhiên liệu hợp lí và tiết kiệm năng lượng là cách bảo vệ môi trường hiệu quả?
IV. Điều chế oxi. Phản ứng phân hủy
1. Điều chế oxi trong phòng thí nghiệm
Cho một lượng nhỏ thuốc tím (![]() ) vào ống nghiệm, nung nóng trên ngọn lửa đèn cồn.
) vào ống nghiệm, nung nóng trên ngọn lửa đèn cồn.
Đưa que đóm còn tàn đỏ vào miệng ống nghiệm.
Nêu hiện tượng và giải thích.
Lời giải
Hiện tượng: Que đóm bùng cháy.
Giải thích: Do phản ứng sinh ra khí oxi duy trì sự cháy.
![]()
Quan sát hình và cho biết tên cách thu khí oxi (phương pháp đẩy nước, đẩy không khí). Giải thích
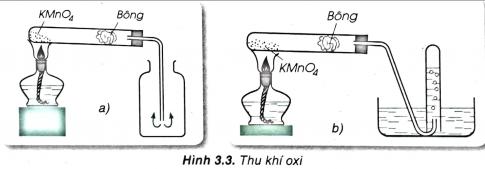
Vậy trong phòng thí nghiệm người ta điều chế oxi như thế nào?
Điền từ hoặc cụm từ cho dưới đây để hoàn thành kết luận về cách điều chế oxi trong phòng thí nghiệm.
(1) chứa oxi, giàu oxi, có nguyên tố oxi.
(2) dễ bị phân hủy ở nhiệt độ cao, dễ bị phân hủy ở nhiệt độ thấp, dễ bị phân hủy ở nhiệt độ thường.
Trong phòng thí nghiệm, khí oxi được điều chế bằng cách nung nóng những hợp chất ![]() và ...(2)... như
và ...(2)... như ![]() ,
, ![]() .
.
2. Phản ứng phân hủy
Hãy điền vào chỗ trống trong các cột ứng với các phản ứng sau:
| Phản ứng hóa học | Số chất phản ứng | Số chất sản phẩm |
| (1) | ||
| (2) | ||
| (3) |
So sánh điểm giống và khác nhau về số chất tham gia phản ứng và số chất sản phẩm trong các phản ứng hóa học trên.
Điền từ/ cụm từ dưới đây để hoàn thành định nghĩa về phản ứng phân hủy
(1) một chất, hai chất, nhiều chất.
(2) một chất mới, hai chất mới, hai hay nhiều chất mới.
Phản ứng phân hủy là phản ứng hóa học trong đó ![]() sinh ra ...(2)...
sinh ra ...(2)...
Lời giải
(1) một chất
(2) hai hay nhiều chất mới
V. Không khí. Sự cháy
1. Thành phần của không khí
a) Thí nghiệm xác định thành phần của không khí
Oxi chiếm bao nhiêu phần trăm thể tích của không khí? Khí không cháy còn lại là bao nhiêu phần trăm?
b) Ngoài khí oxi và nito, không khí còn chứa những chất gì khác?
Tìm dẫn chứng nêu rõ trong không khí có chứa một ít hơi nước.
c) Nguyên nhân gây ô nhiễm không khí và biện pháp bảo vệ không khí trong lành, tránh ô nhiễm

Các hình ảnh trên cho thấy không khí bị ô nhiễm do những nguyên nhân nào
Tác hại của ô nhiễm không khí là gì?
Biện pháp bảo vệ không khí trong lành là gì?
2. Sự cháy và sự oxi hóa chậm
a) Sự cháy
Sự cháy của một chất trong không khí và trong oxi có gì giống và khác nhau? Giải thích.
b) Sự oxi hóa chậm
Hãy tìm các ví dụ về hiện tượng tự bốc cháy.
3. Điều kiện phát sinh và các biện pháp để dập tắt sự cháy
Muốn dập tắt ngọn lửa do xăng dầu cháy, người ta thường trùm vài dày hoặc phủ cát lên ngọn lửa mà không dùng nước. Giải thích.
C. Hoạt động luyện tập
1. Người ta phải sử dụng bình oxi để thở trong những trường hợp nào?
2. Khi tiếp thêm củi vào bếp lửa, cách làm nào sau đây làm cho lửa mạnh hơn. Giải thích
Cách 1: Cho thanh củi to vào bếp
Cách 2: Chẻ mỏng nó ra rồi cho vào bếp
Cách 3: Thổi hoặc quạt thêm không khí vào.
3. Hãy viết PTHH của các phản ứng khi cho oxi tác dụng với: canxi, nhôm, kẽm, đồng, cacbon, lưu huỳnh, photpho (ghi rõ điều kiện phản ứng nếu có)
4. Trong khí (gas) thường dùng có thành phần chính là khí propan (![]() ) và butan (
) và butan (![]() ).
).
a) Viết PTHH của phản ứng xảy ra ở điều kiện thường khi đốt cháy hết khí (gas) giả thiết rằng sản phẩm cháy chỉ gồm ![]() và
và ![]() .
.
b) Tính thể tích ![]() thoát ra ở điều kiện thường khi đốt cháy hết 1 kg gas có thành phần chứa 26,4 % propan và 69,6 % butan, còn lại là tạp chất trơ không cháy (cho rằng 1 mol khí chiếm 24 lít trong điều kiện thường).
thoát ra ở điều kiện thường khi đốt cháy hết 1 kg gas có thành phần chứa 26,4 % propan và 69,6 % butan, còn lại là tạp chất trơ không cháy (cho rằng 1 mol khí chiếm 24 lít trong điều kiện thường).
Lời giải
a) PTHH:
![]()
![]()
b) Số mol của propan và butan trong 1kg khí ga là:
![]()
![]()
Số mol khí cacbonic thu được là: ![]()
Vậy số lít khí cacbonic thu được là: V = 66 × 24 = 1584 (lít).
5. Một buổi làm thực hành thí nghiệm cần 12 lọ oxi, mỗi lọ có dung tích khoảng 200 ml (ở điều kiện thường). Tính khối lượng ![]() tối thiểu cần dùng để thu được lượng oxi trên (cho rằng 1 mol chiếm thể tích 24 lít ở điều kiện thường và không có sự hao hụt trong quá trình điều chế khí).
tối thiểu cần dùng để thu được lượng oxi trên (cho rằng 1 mol chiếm thể tích 24 lít ở điều kiện thường và không có sự hao hụt trong quá trình điều chế khí).
6. Hãy tưởng tượng mình là nguyên tố Oxi, hãy giới thiệu về bản thân mình.
7. Đọc những thông tin trong biểu đồ sau và cho biết ngoài các ứng dụng đã nêu, oxi còn có những ứng dụng gì?
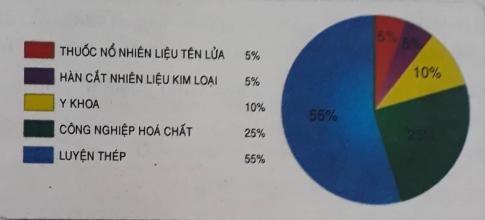
D. Hoạt động vận dụng
1. Người ta ví "Cây xanh là nhà máy sản suất gluxit (cacbonhidrat) và oxi, đồng thời điều hòa lượng oxi trong khí quyển". Bạn hãy giải thích ý kiến đó bằng phương trình hóa học.
Tính thể tích khí cacbonic mà cây xanh đã hấp thụ được bằng quá trình quang hợp nếu quá trình đó giải phóng 134,4 ![]() khí oxi (đktc). Hiệu suất của quá trình tổng hợp đạt 80%. Từ đó em hãy nêu một hành động thiết thực nhất tại ra đình để góp phần bảo vệ môi trường
khí oxi (đktc). Hiệu suất của quá trình tổng hợp đạt 80%. Từ đó em hãy nêu một hành động thiết thực nhất tại ra đình để góp phần bảo vệ môi trường
2. Trong đời sống hằng ngày, những quá trình nào sinh ra khí ![]() , quá trình nào tiêu thụ khí
, quá trình nào tiêu thụ khí ![]() sinh ra khí
sinh ra khí ![]() ?
?
E. Hoạt động tìm tòi mở rộng
1. Em hãy tìm hiều về sự ô nhiễm không khí (Ô nhiễm không khí là gì? Nguyên nhân, tác hại và các biện pháp nhằm giảm sự ô nhiễm không khí).
2. Em hãy tìm hiểu về khả năng oxi kết hợp với chất hemoglobin trong máu.
Giải Khoa học tự nhiên 8 bài 3 sách VNEN trang 14 - Oxi - Không khí được Khoahoc chia sẻ trên đây. Các câu hỏi, bài tập có trong bài học được giáo viên KhoaHoc giải đáp chi tiết, chính xác, rõ ràng theo khung chương trình SGK môn KHTN lớp 8 nhằm hỗ trợ học sinh hoàn thiện lời giải cho các câu hỏi, bài tập và đạt kết quả cao môn KHTN 8. Ngoài ra các bạn có thể tham khảo thêm chuyên mục tài liệu học tập lớp 8 để có được những tài liệu hữu ích của nhiều môn học khác nhau như: Toán, Văn, Lịch sử- Địa lí,...
Xem thêm bài viết khác
- Bộ đề thi Địa lý lớp 8 học kì 2 năm 2022 Đề thi Địa lý lớp 8 học kì 2
- Đề thi Địa lý lớp 8 học kì 2 Trường THCS Tam Thuấn - Hà Nội năm 2021 - 2022 Đề thi Địa lý lớp 8 học kì 2 - có đáp án
- Bộ đề thi Lịch sử lớp 8 học kì 2 năm 2022 Đề thi Lịch sử lớp 8 học kì 2 năm 2022
- Đề thi Lịch sử lớp 8 học kì 2 Trường THCS Bình Định - Thái Bình năm 2021 - 2022 Đề thi Lịch sử lớp 8 học kì 2
- Bộ đề thi Văn 8 học kì 2 năm 2021 - 2022 Đề thi Văn 8 học kì 2 - có đáp án












 Khoa học tự nhiên 8 VNEN
Khoa học tự nhiên 8 VNEN